
pHは溶液の性質を表す指標の1つで、水素イオン(H+)のモル濃度(正しくは、実効モル濃度)を用いて、以下の式から求めます。水の中では、水素イオンと水酸化物イオン(OH-)の濃度の積は常に一定です。従って、溶液中のH+が増えるとOH-は減り、OH-が増えるとH+が減ります。両者が同じ濃度のときpHは7となり中性を示し、pHが7よりも小さい状態を酸性、7よりも大きい状態をアルカリ性と言います。
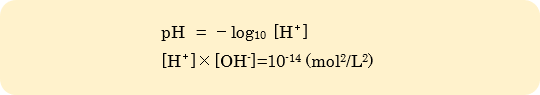
pHは植物の生育環境とも深い関係があります。雨が降ると土壌の成分の一部が溶け出し、溶け出した成分によって酸性からアルカリ性の性質を示します。植物の種類によって好ましい土壌溶液のpHは異なりますが、一般的には弱酸性~中性を好む植物が多く、アルカリ性の土壌では植物が育ちにくいと言われています。土壌の性質は、自然が持って生まれた性質でもありますが、人的な要因で変わることもあります。例えば、軟らかい土地を固くするためにアルカリ性の材料を土に混ぜると、アルカリ成分が溶け出して周辺の植物の生育へ影響を与える可能性があります。pHが変わると様々な物質の溶けやすさも変わるため、元々含まれていた重金属が溶け出して悪影響を及ぼすかもしれません。
私たちの身の回りの物質は、水に触れたり溶かしたりしたときに、様々なpHを示します。 例えば、レモン果汁はpH2程度の酸性を、洗剤はpH10程度のアルカリ性を示します。それでは、ごみを焼却した後の焼却灰が水に触れたときのpHはどれくらいだと思いますか?正解はpH10~12程度のアルカリ性です。焼却灰は、カルシウム等の酸化物を多く含み、水に触れると水酸化カルシウム(Ca(OH)2)に変化して、さらには、Ca2+とOH-となり溶け出すことにより、触れた水のpHをアルカリ性にします。
焼却灰など廃棄物の埋め立てを行っている最終処分場では、焼却灰などから溶け出した色々な成分を含む水が周辺土壌に染み出さないような構造にし、これらの水を集めてきれいに処理をすることで、周辺環境の汚染を防いでいます。これにより、アルカリ性の水も周辺環境に広がることがありません。このような管理を続けるうちに、焼却灰中の成分は雨で洗い流されたり、二酸化炭素と反応して溶けにくい物質に変化したりすることで、水酸化物イオンの溶け出す量は徐々に減ります。しかし、焼却灰中の成分が溶け出し続け、アルカリ性を示す現象が長く続くために、 最終処分場の廃止に係る技術上の基準(1)で定められているpH5.8以上8.6以下(公共用水域に排出する場合)という目標を達成できない施設もあります。このような施設は、最終処分場に焼却灰等を埋め立てた後、しばらく処理やモニタリングなどの管理を続けなければなりません。
最終処分場の廃止に係る技術上の基準(1)で定められているpH5.8以上8.6以下(公共用水域に排出する場合)という目標を達成できない施設もあります。このような施設は、最終処分場に焼却灰等を埋め立てた後、しばらく処理やモニタリングなどの管理を続けなければなりません。
そこで、国立環境研究所では、pHを早く下げるための方法の提案に向けて、焼却灰の溶出試験(2)や表面観察などを行い、様々な角度からアルカリ成分の溶出メカニズムを研究しています。

- (1)環境省_最終処分場維持管理積立金に係る維持管理費用算定ガイドライン_参考資料1
環境省_最終処分場維持管理積立金に係る維持管理費用算定ガイドライン (env.go.jp)- (2)環環_溶出試験の役割と今後の展開 肴倉宏史
循環・廃棄物の基礎講座 [環環 KannKann] - 資源循環・廃棄物研究センター オンラインマガジン (nies.go.jp)
